摘 要:目的 本研究主要通过对罗布麻叶配方颗粒有效成分进行鉴别及测定,建立罗布麻叶配方颗粒质量标准。方法 薄层色谱法(TLC)条件:以甲醇和水饱和正丁醇为提取溶剂,三氯甲烷-甲醇-水-甲酸(7∶2.5∶0.1∶0.2)下层溶液为展开剂,3%三氯化铝乙醇溶液为显色剂,紫外灯(365nm)下检视;高效液相色谱法(HPLC)条件:Kromasil 100-5-C18(250mm×4.6mm,5μm)色谱柱,流动相为乙腈-0.2%磷酸(15∶85),检测波长256nm,进样量10μL,柱温30℃,流速1.0mL/min。结果 对3批样品进行鉴别及测定,薄层色谱斑点清晰;液相色谱方法可靠,可用于罗布麻叶配方颗粒中金丝桃苷的含量测定。结论 该方法准确可靠,可为罗布麻叶配方颗粒质量控制提供科学依据。
关键词:罗布麻叶;金丝桃苷;质量控制
罗布麻叶配方颗粒是夹竹桃科植物罗布麻Apocynu venetum L.的干燥叶经炮制加工后制成的配方颗粒[1]。根据多批次样品的实际性状描述,本品为棕黄色的颗粒,气微,味苦、涩。罗布麻作为一味名贵的中草药,全草可入药,其被李时珍写入《本草纲目》[2]以前,就有对罗布麻的记载,例如三国时期陶弘景所著的《名医别录》[3]也有记载罗布麻的根可以入药;《救荒本草》[4]等记载罗布麻叶具有平心悸、止眩晕的作用。现代药理研究[5-8]证明,罗布麻叶的临床效果较好,在降血压、降血脂、保肝、抗抑郁等方面具有十分明显的功效。中药配方颗粒,是指以单味中药饮片为原料,经现代工艺提取、精制而成的一种颗粒状制剂[9]。由于中药配方颗粒具有便携性及易服用性,因此成为近年来的研究热点,但是其在质量方面仍存在无统一标准的问题,产品质量良莠不齐。本研究为了增加配方颗粒工艺的稳定性以及质量的可控性,对罗布麻叶配方颗粒进行质量控制研究,同时为中药配方颗粒质量研究提供科学依据。
1 材料与设备
1.1 材料
罗布麻叶配方颗粒,批号:1907013、1908013、1908023,规格:3g/袋(相当于饮片量10g),济川药业集团有限公司。罗布麻叶对照药材,批号:120979-201505,规格:2g/支,中国食品药品检定研究院。金丝桃苷,批号:111521-201809,规格:20mg/支,纯度:94.9%,中国食品药品检定研究院。槲皮素,批号:100081-201610,规格:100mg/支,纯度:99.1%,中国食品药品检定研究院。山柰素,批号:110861-202013,规格:20mg/支,纯度:93.2%,中国食品药品检定研究院。糊精,190211,安徽山河药用辅料股份公司。乙醇、乙醚、乙酸乙酯、三氯甲烷、甲酸、磷酸、无水氯化铝为分析纯,上海国药集团。甲醇、乙腈为色谱纯,德国默克公司。
1.2 仪器设备
硅胶G薄层板,青岛海浪硅胶干燥剂有限公司;XSE 205DU电子天平,梅特勒-托利多(常州)称重设备系统有限公司;SY8200T超声波清洗器,上海声源有限公司;Goodlook-2000薄层成像仪,大昌华嘉商业(中国)有限公司;KW-1000DC水浴锅,江苏中大有限公司;SHIMADZU LC20AD高效液相色谱仪,日本岛津公司。
2 方法
2.1 薄层鉴别
2.1.1 鉴别方法
参考《中华人民共和国药典》2020年版第一部中罗布麻叶饮片的薄层鉴别方法并进行优化,该方法分别以罗布麻叶对照药材和槲皮素对照品、山柰素对照品作为对照品。
精密称取罗布麻叶配方颗粒0.3g,置于锥形瓶中,加甲醇溶液20mL,超声处理25min(功率200W,频率58kHz),滤过,滤液蒸干,残渣加水20mL使溶解,用水饱和正丁醇20mL振摇提取,分取正丁醇溶液,置水浴锅上蒸干,残渣加甲醇1mL使溶解,作为供试品溶液。取罗布麻叶对照药材1g,同供试品溶液制备方法处理对照药材,作为罗布麻叶对照药材溶液。取槲皮素对照品、山柰素对照品适量,加乙醇制成每lmL各含0.5mg的溶液,作为对照品溶液。
吸取2μL槲皮素对照品、2μL山柰素对照品溶液、5μL罗布麻叶对照药材溶液、3μL供试品溶液,依次点于同一硅胶G薄层板上,展开剂为三氯甲烷-甲醇-水-甲酸(7∶2.5∶0.1∶0.2),显色剂为3%三氯化铝乙醇溶液,展开晾干喷显色剂后放置于105℃烘箱中加热2min,斑点显色清晰后取出,置紫外灯(365nm)下检视。
2.1.2 专属性试验
精密称取糊精0.015g,置于锥形瓶中,按罗布麻叶供试品处理方法制得阴性样品。分别取槲皮素和山柰素对照品溶液各2μL、罗布麻叶对照药材溶液5μL、供试品和阴性样品溶液各3μL,按优化后的薄层鉴别方法进行操作。
2.1.3 样品鉴别
精密称取3批罗布麻叶配方颗粒0.3g,分别置于锥形瓶中,按优化后的薄层鉴别方法进行操作。
2.2 含量测定
2.2.1 色谱条件
岛津20AD高效液相色谱仪,Kromasil100-5-C18(250mm×4.60mm,5μm)色谱柱,以乙腈-0.2%磷酸(15∶85)为流动相,检测波长为256nm,进样量为10μL,柱温30℃,流速1.0mL/min。
2.2.2 供试品溶液制备
取本品约0.2g,精密称定,置50mL容量瓶中,加50%甲醇适量,超声处理30min,放冷,用50%甲醇定容,摇匀,取上清液滤过,取续滤液,即得。
2.2.3 专属性试验
取糊精0.015g,按“2.2.2”项下供试品溶液制备方法制得阴性样品溶液,分别精密吸取供试品溶液、阴性样品溶液各10μL,注入高效液相色谱仪。
2.2.4 线性关系试验
精密称取金丝桃苷对照品,置20mL容量瓶中,加甲醇溶解并定容至刻度,摇匀,浓度720μg/mL,作为母液。分别精密量取母液5份,置于容量瓶中,加甲醇稀释100、50、20、10、5倍,摇匀,配制成浓度依次递增的对照品溶液。分别精密吸取上述5种浓度的对照品溶液各10μL,注入高效液相色谱仪。
2.2.5 进样精密度试验
精密吸取同一金丝桃苷对照品溶液10μL,注入高效液相色谱仪,连续进样6次。
2.2.6 重复性试验
取同一批样品,按“2.2.2”项下供试品溶液的制备方法平行处理6份,精密吸取各10μL,注入高效液相色谱仪。
2.2.7 稳定性试验
取同一金丝桃苷对照品溶液,分别于0、2、4、6、8、12、18、24h进样,测定金丝桃苷峰面积的RSD值;取同一罗布麻叶配方颗粒供试品溶液,分别于0、2、4、8、12、18、24h精密吸取10μL,注入高效液相色谱仪,测定金丝桃苷峰面积的RSD值。
2.2.8 加样回收试验
精密称取金丝桃苷对照品15mg,置20mL容量瓶中,加甲醇溶解并定容至刻度,即得对照品溶液。取罗布麻叶配方颗粒约0.1g,共6份,精密称定,置于50mL容量瓶中,分别精密加入上述金丝桃苷对照品溶液1mL,再加入适量50%甲醇,超声处理(功率200W,频率58kHz)30min,放冷,加50%甲醇定容,摇匀,滤过,制得6份供试品溶液,精密吸取各10μL,注入高效液相色谱仪。
2.2.9 中间精密度试验
取同一批罗布麻叶配方颗粒,按“2.2.2”项下供试品溶液制备方法处理样品,由不同的操作人员、不同时间、在不同仪器上,按“2.2.1”项下色谱条件进行测定。2.2.10样品测定取3批不同批次的罗布麻叶配方颗粒,按“2.2.2”项下供试品溶液制备方法处理样品,按上述含量测定方法学的结果进行金丝桃苷含量的测定。
3 结果与讨论
3.1 薄层鉴别结果
3.1.1 薄层鉴别方法优化
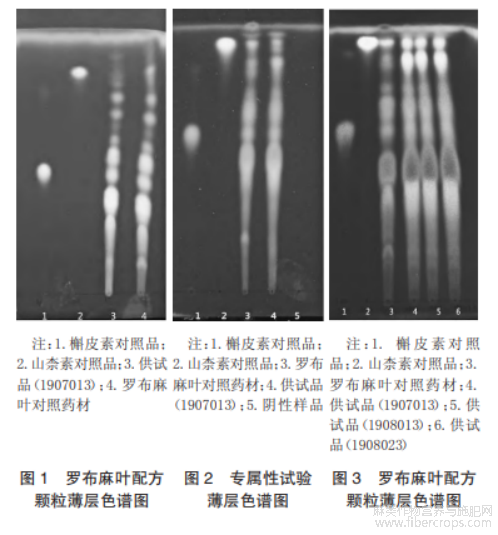
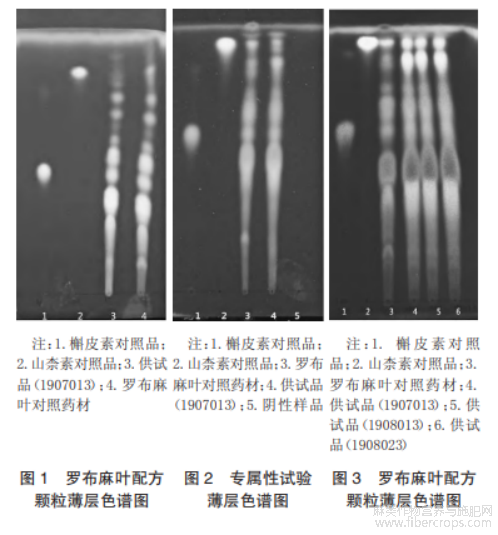
使用《中华人民共和国药典》2020年版一部中罗布麻叶饮片的薄层鉴别方法来鉴别罗布麻叶配方颗粒,虽能有效鉴别出与罗布麻叶对照药材、槲皮素对照品、山柰素对照品相应位置的荧光斑点,但该种方法供试品处理过程繁琐,所用试剂多为乙醚、乙酸乙酯等有毒试剂,故本试验以操作简便和无毒环保为前提,参考了谢思敏等[10]的鉴别方法对罗布麻叶薄层鉴别的处理方法进行优化,选择合适的展开剂,并将罗布麻叶对照药材、槲皮素对照品、山柰素对照品、供试品点于同一硅胶板上进行显色。供试品色谱与对照药材和2个对照品色谱相应位置,有相同颜色的荧光斑点出现(见图1)。且为了排除糊精对罗布麻叶配方颗粒薄层鉴别干扰的可能性,进行了专属性试验,未发现糊精在与对照药材和2个对照品色谱相应位置有相同颜色的荧光斑点(见图2),排除了糊精对本品薄层鉴别的干扰。
3.1.2 样品检测
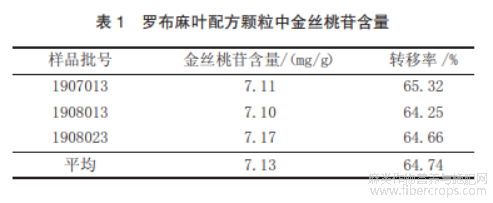
使用上述优化方法对3批罗布麻叶配方颗粒进行薄层鉴别,3批供试品与对照药材、槲皮素对照品、山柰素对照品在相应的位置均有相同颜色的荧光斑点出现(见图3)。所以可将该薄层色谱方法列入罗布麻叶配方颗粒薄层色谱的质量研究中。
3.2 含量测定结果
3.2.1 方法学
金丝桃苷是罗布麻叶配方颗粒的有效活性物质之一,也是《中华人民共和国药典》2020年版中罗布麻叶饮片的含量测定所要求的物质,为考察辅料糊精是否会干扰金丝桃苷的含量测定,从原处方中去除罗布麻叶,按制剂工艺制备得阴性制剂,按供试品溶液制备方法制得阴性样品溶液。对比供试品以及阴性样品色谱图,结果显示阴性样品色谱图在金丝桃苷相应的保留时间处无吸收峰,表明糊精对罗布麻叶配方颗粒含量测定无干扰,该方法专属性较好。
线性关系试验中,以进样浓度(μg/mL)为横坐标,峰面积为纵坐标,绘制标准曲线,所得回归方程为Y=28965.5382X+10078.9254,R2=0.9999。以上表明,金丝桃苷在6.794~135.880μg/mL的浓度范围内呈良好的线性关系。
进样精密度试验中,对照品峰面积RSD值为0.79%,表明该方法进样精密度良好。
重复性试验中,6份样品含量测定结果的RSD值为0.64%,表明该方法重现性较好。
稳定性试验中,对照品峰面积RSD值为0.80%,供试品峰面积RSD为0.21%,表明对照品溶液以及供试品溶液在24h内稳定性良好。
加样回收试验中,平均加样回收率为95.44%,RSD值为1.40%,说明该方法准确度较好。
中间精密度试验中,中间精密度RSD值为1.40%,表明该方法中间精密度良好。
以上含量测定方法学试验表明,罗布麻叶配方颗粒中金丝桃苷的含量测定方法的专属性强,进样精密度、重复性、稳定性等均符合规定,故此高效液相色谱条件可用于罗布麻叶配方颗粒中的金丝桃苷的含量测定。
3.2.2 样品测定
取罗布麻叶配方颗粒(批号:1907013、1908013、1908023),按上述含量测定方法检测,罗布麻叶配方颗粒的金丝桃苷的平均含量为7.13mg/g,平均转移率为64.74%。测定结果见表1。
3.3讨论
薄层色谱鉴别试验中,前期研究对供试品点样量1μL、3μL、5μL进行了考察,发现点样量过大易造成主要荧光斑点过大而聚集在一起,不易鉴别,点样量过小易造成荧光斑点不清晰,而点样量为3μL时,荧光斑点较为适宜,故最终选择3μL的点样量。
含量测定方法学试验中,对超声提取、加热回流提取2种不同方式进行了考察,结果发现超声提取方式效率高且易操作,故选择超声提取;考察了30%甲醇、50%甲醇、70%甲醇和相同浓度的乙醇不同提取溶剂对含量测定的影响,结合《中华人民共和国药典》2020年版中50%甲醇提取溶剂,仍采用50%甲醇作为提取溶剂;考察了25mL、50mL、70mL等提取溶剂量对含量测定的影响,结果发现不同提取溶剂量所测含量差异无显著性,考虑到对照品与样品峰面积不易过大且溶剂使用量最少的原则,选择50mL作为最佳提取溶剂量;考察了15min、30min、45min3个不同提取时间对含量测定的影响,结果显示超声提取30min时所测金丝桃苷含量最大,故选择超声提取30min。
中药配方颗粒作为中药饮片的补充,质量标准应充分考虑中药配方颗粒与中药饮片基本属性的一致性[11]。本研究采用薄层色谱法对罗布麻叶配方颗粒进行鉴别,供试品与罗布麻叶对照药材、槲皮素对照品、山柰素对照品相应的位置上,显相同颜色的荧光斑点。该方法较《中华人民共和国药典》2020年版中薄层鉴别方法便于操作,且鉴别效果好,适用于生产实践中。采用高效液相色谱法对金丝桃苷含量测定,方法学试验结果均符合规定,并用此方法对3批罗布麻叶配方颗粒进行测定,金丝桃苷平均含量为7.13mg/g,转移率平均值为64.74%。《中华人民共和国药典》2020年版一部罗布麻叶饮片项下规定金丝桃苷的含量不得少于0.30%,按照转移率按平均值±30%(即45.32%~84.16%)作为限度范围,则罗布麻叶配方颗粒中含金丝桃苷的含量范围为4.53~8.42mg/g(每袋3g,相当于饮片量10g),故暂定罗布麻叶配方颗粒的含量限度为:本品每1g含罗布麻叶以金丝桃苷(C21H20O12)计应为4.53~8.42mg/g。
4 结论
本试验主要从薄层鉴别方法以及含量测定方法2个方面制定罗布麻叶质量标准。薄层鉴别方法中,以甲醇及水饱和正丁醇为提取溶剂,以三氯甲烷-甲醇-水-甲酸(7∶2.5∶0.1∶0.2)为展开剂,以3%三氯化铝乙醇为显色剂,供试品与对照药材、槲皮素对照品、山柰素对照品在相应的位置均有相同颜色的荧光斑点出现;含量测定方法中,色谱条件为岛津20AD高效液相色谱仪,Kromasil 100-5-C18(250mm×4.60mm,5μm)色谱柱,以乙腈-0.2%磷酸(15∶85)为流动相,检测波长为256nm,进样量为10μL,柱温30℃,流速1.0mL/min。在此色谱条件下,测定的罗布麻叶配方颗粒的金丝桃苷平均含量为7.13mg/g,暂定罗布麻叶配方颗粒的含量限度为:本品每1g含罗布麻叶以金丝桃苷(C21H20O12)计应为4.53~8.42mg/g。
参考文献
[1] 国家药典委员会.中华人民共和国药典:一部[S].北京:中国医药科技出版社,2020:211.
[2] 明·李时珍.本草纲目[M].金陵版点校本.陈贵廷,等,点校.北京:中医古籍出版社,1994:363-365.
[3] 梁·陶弘景.名医别录[M].尚志钧,辑校.北京:人民卫生出版社, 1986.
[4] 朱橚.景印文渊阁四库全书.救荒本草[M].影印本.台北:台湾商务印书馆,1986:771.
[5] 李芝,王超云,张树平,等.罗布麻叶总黄酮对高脂高盐大鼠高血压的影响及其分子机制[J].中草药,2012,43(3):540-545.
[6] 张素琼,燕虹,李青山.罗布麻叶有效部位降血脂及抗动脉粥样硬化的研究[J].中西医结合心脑血管病杂志,2007,5(9):831-832.
[7] 于鸣兰.罗布麻叶等中药中化学成分的分离分析[D].聊城:聊城大学,2014.
[8] 郑梅竹.罗布麻叶总黄酮抗抑郁作用及其机制研究[D].长春:吉林大学,2011.
[9] 王一战,苏芮,韩经丹,等.中药配方颗粒的发展现状及思考[J].上海中医药杂志,2016,50(11):10-13.
[10] 谢思敏,侯惠婵,顾利红,等.真伪罗布麻叶的薄层色谱鉴别研究[J]. 今日药学,2019,29(5):318-320,343.
[11] 何军,朱旭江,杨平荣,等.中药配方颗粒的现状与发展新思路[J]. 中草药,2018,49(20):4717-4725.
文献摘自:吴艳芳,秦海军,俞周萍,于波,王靖婷,黄杨敏,沈治平,李超.罗布麻叶配方颗粒质量控制研究[J].中国中医药现代远程教育,2023,21(05):147-150.