摘 要:利用添加了不同量(40、80mg/kg)的外源镉(Cd)的土壤(有效Cd质量分数分别为17.40、51.50mg/kg)进行亚麻盆栽试验,研究不同水平Cd处理对亚麻的出苗率、株高、茎粗、叶片数、生物量及不同器官Cd含量等的影响。结果表明:与对照相比,低质量分数Cd(40mg/kg)提高了亚麻的出苗率,而高质量分数Cd(80mg/kg)则抑制了出苗;Cd处理降低了亚麻植株的株高、茎粗和叶片数及生物量,且随着Cd处理水平的提高,亚麻的各种生长指标受抑制程度均显著加重,与对照相比,高质量分数Cd处理的亚麻的株高、茎粗、叶片数等分别降低了64.1%、51.9%和58.6%;在器官水平上,亚麻的根、叶、茎中Cd质量分数依次降低;在亚细胞水平上,Cd更多的分布在细胞壁和核糖体上,且显著高于细胞核与叶绿体、线粒体的。可见,40、80mg/kg的Cd处理会抑制亚麻的生长和生物量的积累,而亚麻对Cd的耐受性可能是根部对Cd向上运输的限制及细胞壁和液泡对Cd的隔离所致。
关键词:亚麻;土壤;镉;生物量;亚细胞;耐镉机制
在人类活动因素和自然因素双重作用下,土壤、水体中的重金属污染情况日益严重[1–2],严重制约着中国农业可持续发展。在诸多有害重金属中,镉(Cd)因其移动性强、毒性高、易随食物链累积而备受关注[3–5],土壤Cd污染修复任务紧迫。在各种修复手段中,植物修复模式因具有环保、成本低、易操作等优点而成为研究的热点。寻找适合Cd污染农田修复和利用的作物,一直是科研工作者的目标之一。
亚麻是世界三大纤维和五大油料作物之一,是人类最早栽培的古老作物[6]。亚麻有200多个品种,根据其用途分为纤维用、油用、油纤兼用3种类型[7]。随着对亚麻研究的扩展和深入,亚麻在生物复合材料[8]、医用[9]等领域的利用已取得了较大进展,这使得亚麻的经济利用价值更加突出。此外,人们还发现亚麻对Cd具有很好的吸收能力和耐性,如GUO等[10]发现,一些亚麻品种每年每公顷可在土壤中移除60g的Cd,而BJELKOVÁ[11]则发现,某些亚麻品种在Cd含量为1000mg/kg的土壤上依然可正常生长。同时,种植在Cd污染农田上的亚麻还可作为能源作物用于生物燃料的生产[12]。可见,亚麻有潜力去替代那些经济利用价值低、生长缓慢、生物量小的超积累植物来实现Cd污染土壤的修复和利用[13]。
关于用亚麻修复Cd污染农田的研究较多,但大多数集中于高富集Cd的亚麻品种筛选、亚麻对Cd的修复效果及亚麻对Cd胁迫生理响应等,而对生存在Cd胁迫下的亚麻体内积累的Cd的亚细胞水平的分布情况研究较少。本研究中,探究不同水平Cd处理对亚麻植株形态学的影响,进入亚麻植株体内的土壤Cd在亚麻根、茎、叶等器官内的分布情况及根、茎、叶等器官内的Cd在亚细胞水平上的分布情况。现将结果报告如下。
1材料与方法
1.1供试土壤与亚麻品种
供试土壤采集于湖南省益阳市沅江市。土壤有机质和全氮质量分数分别为26.9、1.31g/kg;有效磷和速效钾质量分数分别为40.0、91.5mg/kg;pH为7.35。
供试亚麻品种为中国农业科学院麻类研究所选育的中亚1号,是中早熟纤维用亚麻品种。其株高约95~105cm,原茎产量依据不同产地情况可达6~11t/hm2,适合中国绝大部分产区种植,具有较强的抗倒伏品质。研究[10]表明,中亚1号对Cd具有较好的耐性和修复效果。
1.2 试验设计
去除在田间采集的土壤样品中的大石块、植物残体等,风干后过2mm筛,然后对土壤样品进行3种处理:不加Cd的对照(CK)、添加40mg/kg的低Cd处理(Cd40)和添加80mg/kg的高Cd处理(Cd80),其土壤有效Cd质量分数分别为0.14、17.40、51.50mg/kg。由于在之前的田间试验中发现亚麻在自然环境中各种Cd污染程度下的农田里均可较好的生长,本试验设计了更高浓度的Cd处理,以便检验亚麻的耐Cd潜力及Cd在亚麻植株内的积累、分布情况。将处理好的土壤分别装入花盆中,静置2月,使加入的Cd达到转化平衡。2月后,在每盆中加入适量的水,将花盆中土壤的含水量调整为田间持水量的70%,再将70粒亚麻种子播种在表层土下2cm深度处。每周观察2次亚麻出苗及长势情况。及时喷水,避免土壤干燥,治虫和除草视情况而定。
1.3测定项目及方法
1.3.1亚麻的形态指标和生物量测定
播种2周后,计数每个处理的亚麻苗数,并计算出苗率。播种40d后收获亚麻,在每盆亚麻苗中选取10株测定其株高、茎粗和叶片数;然后用蒸馏水洗净每盆的植株,并在吸干植株表面的水分后称其鲜质量;再取部分植株进行烘干,测定植株的含水率,进而根据含水率计算每盆亚麻植株的干生物量。
1.3.2亚麻亚细胞组分的分离及 Cd 含量的测定
取部分洗净并吸干植株表面水分的新鲜亚麻苗,将其分为根、茎和叶,采用差速离心法对此3部位的细胞进行亚细胞器分离,具体操作流程参照李德明等[14]和SUN等[15]的方法并有所改进。称取0.5g样品于研钵中,加入20mL预冷的pH7.4的亚细胞缓冲溶液(250mmol/L蔗糖、1mmol/L二硫赤藓醇、50mmol/LTris–HCl),迅速将样品研磨成匀浆。对所得匀浆进行差速离心:以300r/min的速度离心30s,沉淀为细胞壁组分;上层清液再以2000r/min的速度离心15min,沉淀为细胞核和叶绿体组分;上层清液再以10000r/min的速度离心20min,沉淀为线粒体组分;其余上清液为可溶性部分,包括核糖体等。上述所有步骤均在4℃条件下进行。用去离子水洗涤细胞壁组分,过滤后将滤渣转移至消煮管,其余组分分别用去离子水洗入消煮管,60℃烘干后,用体积比为5∶1的硝酸、高氯酸消解,最后采用ICP–MS测定Cd的含量。利用亚麻植株不同部位的4个亚细胞组分的Cd含量分别计算亚麻植株不同部位的Cd含量。
1.4数据处理
数据均使用Microsoft Excel 2016进行整理;运用SPSS 22.0进行方差分析,采用Duncan法在P<0.05的显著水平上进行多重比较。
2结果与分析
2.1Cd处理对亚麻植株形态及生物量的影响
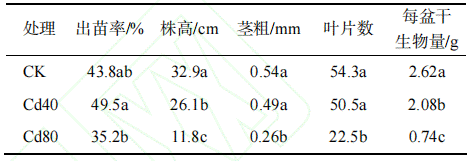
Cd处理可影响亚麻的出苗率、株高、茎粗、叶片数,最终影响亚麻的生物量,但Cd对亚麻的影响因质量分数不同而存在差异(表1)。从表1可以看出,Cd40对亚麻的出苗有一定的促进作用,Cd40的出苗率较CK的提高了13.0%;Cd80的出苗率较CK的降低了19.6%,但差异无统计学意义;Cd80的出苗率显著低于Cd40的。Cd的存在对亚麻产生了不同程度的毒害作用,不论何种质量分数的Cd处理都会影响亚麻的株高、茎粗和叶片数。与CK相比,Cd40在一定程度上降低了亚麻的株高、茎粗和叶片数,分别降低了20.7%、9.3%和7.0%;而Cd80则无一例外地显著降低了亚麻的株高、茎粗和叶片数,分别降低达64.1%、51.9%和58.6%。Cd的存在不仅影响了亚麻植株形态,也显著影响了亚麻的生物量。与CK相比,2种水平的Cd处理均显著降低了亚麻的生物量,且随着Cd质量分数的增加,亚麻生物量的降低更加明显,Cd40和Cd80的生物量分别降低了20.6%和71.8%。
表1 Cd处理下亚麻的出苗率和植株形态特征及生物量
同列不同字母示处理间差异有统计学意义(P<0.05)。
2.2Cd处理下亚麻植株内 Cd 的含量与分布
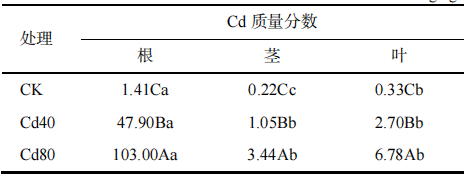
从表2可以看出,土壤中的Cd经亚麻根系吸收后会进入亚麻体内进行再分布,并且在亚麻体内各个器官中的分布差异明显,根、叶、茎中Cd的质量分数依次降低,其中,根中的Cd质量分数显著高于叶和茎的,且随着土壤Cd质量分数的增加亚麻植株各器官的Cd质量分数也显著增加。
表2 Cd处理下亚麻的根和茎及叶中的Cd 质量分数
同列不同大写字母示处理间差异有统计学意义(P<0.05);同行不同小写字母示器官间差异有统计学意义(P<0.05)。
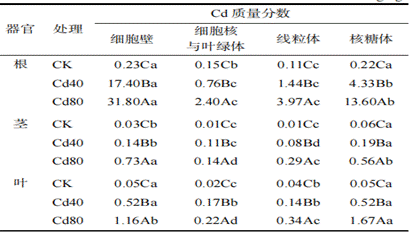
从表3可以看出,在3个器官中,在亚麻亚细胞水平上细胞壁和核糖体组分的Cd质量分数较高,显著高于细胞核与叶绿体、线粒体组分的Cd质量分数;随着土壤Cd质量分数的增加,各个器官的各亚细胞组分的Cd质量分数也显著增加;细胞壁和核糖体是细胞内Cd积累的主要位置。
表3 亚麻根和茎及叶在亚细胞水平上的Cd 质量分数
同一器官同列不同大写字母示处理间差异有统计学意义(P<0.05);同行不同小写字母示亚细胞组分间差异有统计学意义(P<0.05)。
3讨论本研究中,低浓度Cd处理可促进亚麻出苗,而高浓度Cd处理抑制亚麻出苗,这与郭媛等[16]的研究结果类似。其原因可能是低浓度Cd处理刺激了亚麻种子内RNA和蛋白质的合成,从而促进了种子的萌发和出苗[17]。与对照相比,Cd处理降低了亚麻的株高、茎粗和叶片数。DOUCHICHE等[18]在向沙培的亚麻品种Hermes施加0.1mmol/L的Cd时,亚麻的株高、茎粗和叶片数也受到了显著的负面影响。本研究结果与其相似。本研究中,Cd处理显著降低了亚麻的生物量,且该影响随着Cd质量分数的增加而增加,这与已报道的研究[19]的结果相似。而导致亚麻生物量降低的原因可能是植株细胞内和分子水平上的一些生理生化过程由于Cd处理而发生了变化[20]。此外,Cd处理下植株体内活性氧的产生会导致调节植物正常功能的各种酶和官能团的堵塞或失活[21],最终抑制植株的光合作用,降低了有机物质的积累。
植
重金属处理时,植物会通过各种途径抵御和减轻重金属对自身的伤害,如最大限度减少重金属的吸收或运输,并通过修饰或隔离进行解毒[23]。了解Cd在亚麻体内亚细胞水平上的浓度和分布可在一定程度上阐明亚麻耐Cd和吸Cd的机制。本研究中,亚麻细胞壁和核糖体组分中Cd的质量分数较高,显著高于细胞核与叶绿体、线粒体组分中的。细胞壁组分的Cd质量分数较高,可能是位于细胞壁上的一些功能集团与Cd发生了螯合,将部分Cd“固定”到了细胞壁上;核糖体组分Cd质量分数高,则可能是此组分汇集了细胞内所有可溶性组分,包括可能对有毒物质进行隔离的液泡等[23]。
4结论
1)当土壤有效Cd质量分数为17.4mg/kg时,Cd会对亚麻出苗产生促进作用,高于此量则可能会抑制亚麻出苗。
2)添加Cd处理,使土壤有效Cd质量分数为51.50mg/kg时,会严重抑制亚麻的生长和生物量积累,形态学上表现为降低株高、茎粗及叶片数等。
3)亚麻根、叶、茎中Cd的质量分数依次降低,而在亚细胞水平上细胞壁和核糖体的Cd质量分数显著高于细胞核与叶绿体、线粒体的。
参考文献
[1]ZHAO H,WEI Y,WANG J,et al.Isolation and expression analysis of cadmium-induced genes from Cd/Mn hyperaccumulator Phytolacca americana in response to high Cd exposure[J].Plant Biology,2019, 21(1):15–24.
[2]CAO X Y,TAN C Y,WU L H,et al.Atmospheric deposition of cadmium in an urbanized region and the effect of simulated wet precipitation on the uptake perfor-mance of rice[J].Science of the Total Environment,2020,700:134513.
[3]CABRAL M,TOURE A,GARÇON G,et al.Effects of environmental cadmium and lead exposure on adults neighboring a discharge:evidences of adverse health effects[J].Environmental Pollution,2015,206:247–255.
[4]YAN H L,XU W X,XIE J Y,et al.Variation of a major facilitator superfamily gene contributes to differential cadmium accumulation between rice subspecies[J].Nature Communications,2019,10:2562.
[5]李陈贞,孙亚莉,刘红梅,等.镉胁迫下不同水稻品种幼苗生长及光合性能的差异[J].湖南农业大学学报(自然科学版),2021,47(2):147–152.
[6]WANG Y F,JANKAUSKIENE Z,QIU C S,et al.Fiber flax breeding in China and Europe[J].Journal of Natural Fibers,2018,15(3):309–324.
[7]龚静.干旱胁迫和复水对亚麻生长发育及其产量的影响[D].重庆:西南大学,2016.
[8]BARKOULA N M,GARKHAIL S K,PEIJS T.Biode-gradable composites based on flax/polyhydroxybutyrate and its copolymer with hydroxyvalerate[J].Industrial Crops and Products,2010,31(1):34–42.
[9]PRASAD K.Antioxidant activity of secoisolariciresinol diglucoside-derived metabolites,secoisolariciresinol, enterodiol,and enterolactone[J].The International Journal of Angiology:Official Publication of the International College of Angiology,Inc,2000,9(4):220–225.
[10]GUO Y,QIU C S,LONG S H,et al.Cadmium accumulation,translocation,and assessment of eighteen Linum usitatissimum L.cultivars growing in heavy metal contaminated soil[J].International Journal of Phytoreme-diation,2020,22(5):490–496.
[11]BJELKOVÁ M,GEN?UROVÁ V,GRIGA M.Accumu-lation of cadmium by flax and linseed cultivars in field-simulated conditions:a potential for phytoremediation of Cd-contaminated soils[J].Industrial Crops and Products, 2011,33(3):761–774.
[12]SHI G R,CAI Q S.Cadmium tolerance and accumulation in eight potential energy crops[J].Biotechnology Advances, 2009,27(5):555–561.
[13]SALEEM M H,ALI S,HUSSAIN S,et al.Flax(Linum usitatissimum L.):a potential candidate for phytoremediation? Biological and economical points of view[J].Plants, 2020,9(4):496.
[14]李德明,朱祝军.镉在不同品种小白菜中的亚细胞分布[J].科技通报,2004,20(4):278–282.
[15]SUN J L,LUO L Q.Subcellular distribution and chemi- cal forms of Pb in corn:strategies underlying tolerance in Pb stress[J].Journal of Agricultural and Food Chemistry, 2018,66(26):6675–6682.
[16]郭媛,邱财生,龙松华,等.镉胁迫对不同地区亚麻主栽品种种子萌发的影响[J].作物杂志,2015(4): 146–151.
[17]PATRA J,LENKA M,PANDA B B.Tolerance and co- tolerance of the grass Chloris barbata Sw.to mercury, cadmium and zinc[J].New Phytologist,1994,128(1): 165–171.
[18]DOUCHICHE O,CHAÏBI W,MORVAN C.Cadmium tolerance and accumulation characteristics of mature flax,cv.Hermes:contribution of the basal stem compared to the root[J].Journal of Hazardous Materials,2012,235/236:101–107.
[19]AMNA,ALI N,MASOOD S,et al.Differential effects of cadmium and chromium on growth,photosynthetic activity,and metal uptake of Linum usitatissimum in association with Glomus intraradices[J].Environmental Monitoring and Assessment,2015,187(6):311.
[20]SHANKER A K,CERVANTES C,LOZA-TAVERA H, et al . Chromium toxicity in plants[J] . Environment International,2005,31(5):739–753.
[21]LA ROCCA N,ANDREOLI C,GIACOMETTI G M, et al.Responses of the Antarctic microalga Koliella antarctica(Trebouxiophyceae,Chlorophyta) to cadmium contamination[J] . Photosynthetica , 2009 , 47(3) : 471–479.
[22]BAKER A J M.Metal tolerance[J].New Phytologist,1987,106(Suppl):93–111.
[23]GONG Z Z,XIONG L M,SHI H Z,et al.Plant abiotic stress response and nutrient use efficiency[J].Science China Life Sciences,2020,63(5):635–674.
文章摘自:赵信林,王慧,邱化蛟,邱财生,龙松华,王玉富,郭媛.镉处理对亚麻生长发育的影响及镉在亚麻体内的分布[J/OL].湖南农业大学学报(自然科学版):1-5.
物对重金属的耐受机制包括对重金属的排斥和积累,前者是指植物避免吸收重金属和限制重金属转移到枝叶,具有这类耐受机制的作物表现为根部重金属含量高于地上部重金属含量[22]。土壤中的Cd经亚麻根系吸收后会进入亚麻体内进行再分布,从而导致植株不同器官的Cd含量有所不同[23]。本研究中,亚麻植株的根、叶、茎中Cd的质量分数依次降低。可见,亚麻对Cd的耐受机制应该属于排斥机制。随着土壤Cd含量的增加,亚麻植株各器官的Cd质量分数也显著升高,这与前人的研究结果[12]一致。