摘 要:本发明涉及一种罗布麻叶中的黄酮苷类化合物制备方法和用途,该方法将罗布麻叶药材用乙醇回流提取,经大孔树脂富集后得罗布麻叶总黄酮提取物,再经聚酰胺柱分离以及中试制备液相色谱分离,获得较纯的单体化合物为槲皮素?3?O?(6″?丙二酰基)?,β,?D?葡萄糖苷。经实验表明,本发明所获得的述罗布麻叶中黄酮苷类化合物槲皮素?3?O?(6″?丙二酰基)?,β,?D?葡萄糖苷具有抗炎作用,作为抗炎活性功效的保健品具有很好的应用前景。
1.一种罗布麻叶中的黄酮苷化合物制备方法,其特征在于按下列步骤进行:
a、取罗布麻叶药材,加入5?15倍量体积的30?70%乙醇水溶液,在温度95℃回流提取1?3次,每次提取1?3h,提取后过滤,合并提取液,浓缩至无醇味,得到提取物;
b、将步骤a得到的提取物,使用大孔树脂进行黄酮类成分的富集,上样浓度为0.1?0.3g/mL,药材树脂体积比为1:5?1:10,上样流速为1BV/h?3BV/h,用水洗脱1?3个柱体积,除去水溶性杂质,洗脱液为2?5倍体积的30%?70%乙醇,收集洗脱液,真空干燥后得罗布麻总黄酮有效部位提取物;
c、称取步骤b得到的有效部位提取物,使用聚酰胺填料进行柱分离,上样量与聚酰胺用量质量比为1:20?1:40,洗脱溶剂为体积浓度10%?90%乙醇,梯度洗脱,收集50%?90%乙醇洗脱液,并在温度50℃下用旋转蒸发仪浓缩,真空干燥,得到槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷粗提物;
d、将步骤c得到槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷粗提物加入甲醇溶解,再经中试反相色谱柱色谱分离,色谱条件为:体积比18:82的乙腈?0.1%甲酸水为流动相,流速180mL/min,温度室温,保留时间为18?20min,最后分离得到罗布麻叶中的黄酮苷类化合物,化学名称:槲皮素?3?O?(6″?丙二酰基)?β?D?葡萄糖苷。
2.根据权利要求1所述的罗布麻叶中的黄酮苷类化合物槲皮素?3?O?(6″?丙二酰基)?β?D?葡萄糖苷在制备抗炎活性功效的保健品中的用途。
技术领域
本发明涉及生物医药技术领域,具体涉及一种罗布麻叶黄酮苷类化合物制备方法和用途。
背景技术
炎症(inflammation):具有血管系统的活体组织对损伤因子所发生的防御反应为炎症。血管反应是炎症过程的中心环节。非甾体类抗炎药(NSAIDs)在临床上仍为首选用于炎症,在我国其消耗量仅次于抗感染药。但是,NSAIDs有诸多的不良反应,尤其对消化系统的影响最大。罗布麻叶Apocynum venetum L .为夹竹桃科多年生宿根草本植物罗布麻的干燥叶。《中国药典》中收载罗布麻叶为常用中药,其味甘、苦、性凉,具有平肝安神,清热利水之功效。
罗布麻广泛用于食物和药物中,为不可多得的天然药用植物资源,药理研究表明罗布麻叶具有降血压、降血脂、镇静、利尿、抗衰老、增强免疫力等作用。本课题组研究表明槲皮素?3?O?(6″?丙二酰基)?β?D?葡萄糖苷在罗布麻叶中的活性好,且含量较高,所以通过分离纯化的手段得到槲皮素?3?O?(6″?丙二酰基)?β?D?葡萄糖苷并对其活性进行研究的工作具有重要的意义。槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷是一种黄酮苷类化合物,且至今尚未见关于槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷针对抗炎活性的报道。
本发明目的在于,提供一种罗布麻叶中黄酮苷类化合物的制备方法和用途,该方法将罗布麻叶药材用乙醇回流提取,经大孔树脂富集后得罗布麻叶总黄酮提取物,再经聚酰胺柱分离以及中试制备液相色谱分离,获得较纯的单体化合物为槲皮素?3?O?(6″?丙二酰基)?β?D?葡萄糖苷。经实验表明,本发明所述罗布麻叶中黄酮苷类化合物具有抗炎作用,作为具有抗炎活性功效的保健品,具有很好的应用前景。
本发明所述的一种罗布麻叶中的黄酮苷化合物的制备方法,按下列步骤进行:
a、取罗布麻叶药材,加入5?15倍量体积的30?70%乙醇水溶液,在温度95℃回流提取1?3次,每次提取1?3h,提取后过滤,合并提取液,浓缩至无醇味,得到提取物;
b、将步骤a得到的提取物,使用大孔树脂进行黄酮类成分的富集,上样浓度为0.1?0.3g/mL,药材树脂体积比为1:5?1:10,上样流速为1BV/h?3BV/h,用水洗脱1?3个柱体积,除去水溶性杂质,洗脱液为2?5倍体积的30%?70%乙醇,收集洗脱液,真空干燥后得罗布麻总黄酮有效部位提取物;
c、称取步骤b得到的有效部位提取物,使用聚酰胺填料进行柱分离,上样量与聚酰胺用量质量比为1:20?1:40,洗脱溶剂为体积浓度10%?90%乙醇,梯度洗脱,收集50%?90%乙醇洗脱液,并在温度50℃下用旋转蒸发仪浓缩,真空干燥,得到槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷粗提物;
d、将步骤c得到槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷粗提物加入甲醇溶解,再经中试反相色谱柱色谱分离,色谱条件为:乙腈?0.1%甲酸水18:82为流动相,流速180mL/min,温度室温,保留时间为18?20min,最后分离得到罗布麻叶中的黄酮苷类化合物,化学名称:槲皮素?3?O?(6″?丙二酰基)?β?D?葡萄糖苷。
所述罗布麻叶中的黄酮苷类化合物槲皮素?3?O?(6″?丙二酰基)?β?D?葡萄糖苷在制备具有抗炎活性功效的保健品中的用途。
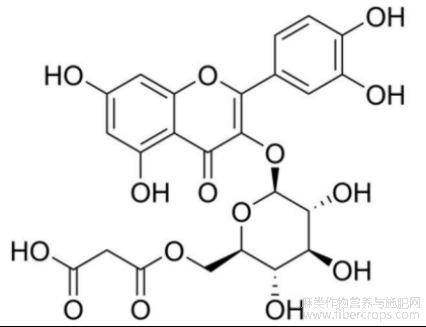
本发明所述的一种罗布麻叶中的黄酮苷类化合物的制备方法,该方法中化合物的化学结构式如下:
其中:化学名称为槲皮素?3?O?(6″?丙二酰基)?β?D?葡萄糖苷。
通过本发明所述方法获得的罗布麻叶中的黄酮苷类化合物槲皮素?3?O?(6″?丙二酰基)?β?D?葡萄糖苷在保健品中的应用。经药理研究表明,本发明所提供罗布麻叶中的黄酮苷类化合物槲皮素?3?O?(6″?丙二酰基)?β?D?葡萄糖苷可显著降低小鼠单核巨噬细胞(RAW264.7细胞)和小鼠小胶质细胞(BV2细胞)经脂多糖刺激后一氧化氮(NO)的含量,降低脂多糖刺激后小鼠单核巨噬细胞(RAW264.7细胞)中的肿瘤坏死因子?α(TNF?α)和白介素?6(IL?6)含量。说明该化合物具有良好的抗炎作用。有望开发成新的具有抗炎活性功效的保健品。
附图说明
图1为本发明化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷的HPLC图谱;
图1
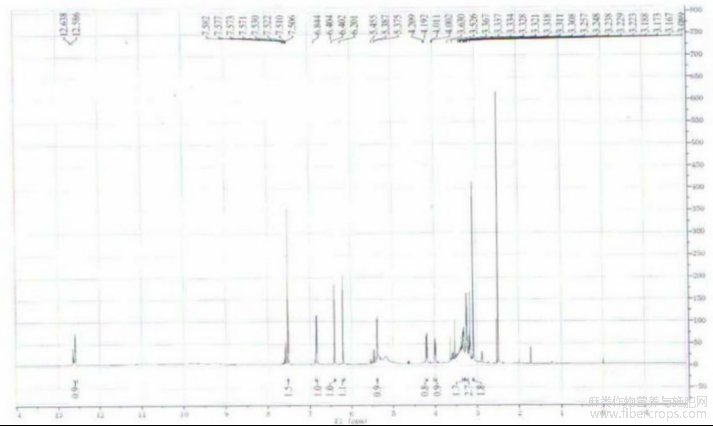
图2为本发明化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷的1HNMR图谱;
图2
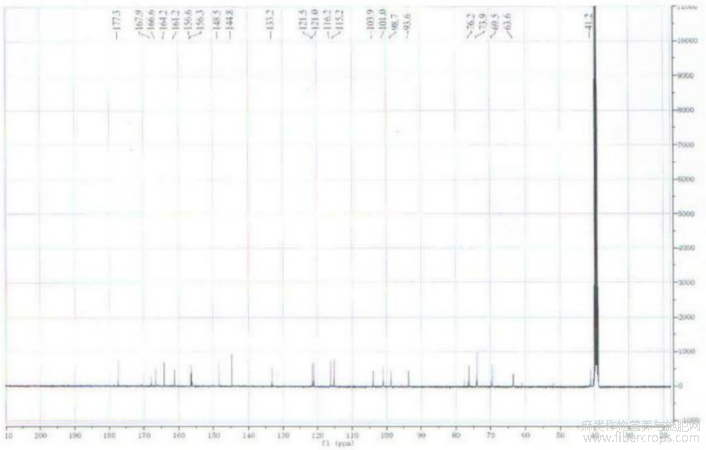
图3为本发明化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷的13CNMR图谱;
图3
图4为本发明不同浓度的化合物对小鼠单核巨噬细胞(RAW264.7细胞)细胞活力的影响图;
图4
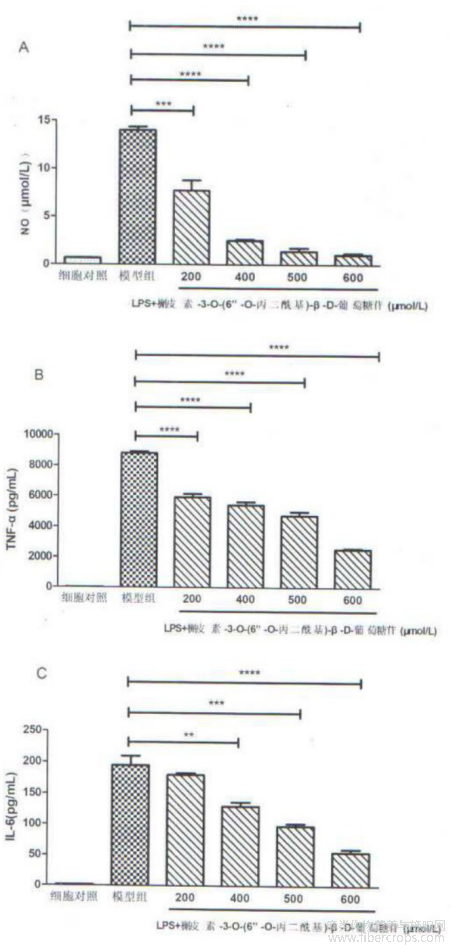
图5为本发明不同浓度的化合物对脂多糖诱导的小鼠单核巨噬细胞(RAW264.7细胞)中一氧化氮(NO)、肿瘤坏死因子?α(TNF?α)和白介素?6(IL?6)含量的影响图:A:对细胞中一氧化氮(NO)的影响;B:对细胞中肿瘤坏死因子?α(TNF?α)含量的影响;C:对细胞中白介素?6(IL?6)含量的影响;其中与模型组比****P<0.0001;***P<0.001;**P<0.01;*P<0.05;
图5
图6为本发明不同浓度化合物对小鼠小胶质细胞(BV2细胞)细胞活力的影响图;
图6
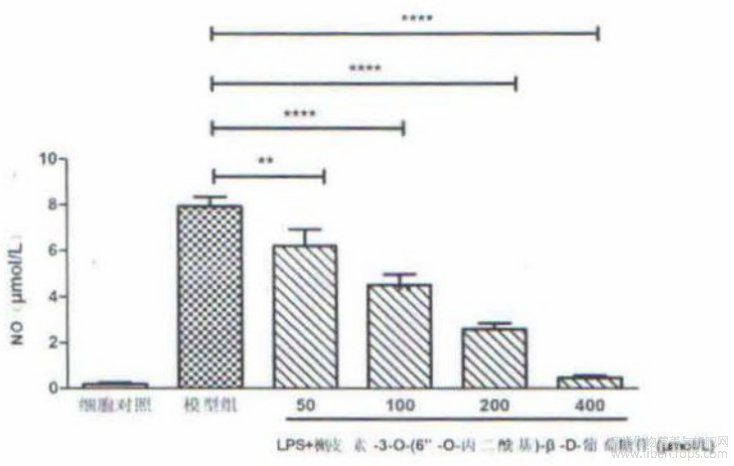
图7为本发明不同浓度化合物对脂多糖诱导的小鼠小胶质细胞(BV2细胞)细胞中一氧化氮(NO)含量的影响图,其中与模型组比****P<0.0001;***P<0.001;**P<0.01;*P<0.05。
图7
具体实施方式
下面结合具体实施例,进一步详细阐述本发明。
实施例1
化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷的制备:
a、取干燥的罗布麻叶药材6kg,加入10倍量体积的浓度50%乙醇水溶液,在温度95℃回流提取3次,每次提取1.5h,提取后过滤,合并提取液,浓缩至无醇味,得提取物2.2kg;
b、取步骤a得到的提取物300g,使用大孔树脂进行黄酮类成分的富集,上样浓度为0.15g/mL,药材树脂体积比为1:5,上样流速为2BV/h,用水洗脱1个柱体积,除去水溶性杂质,洗脱液为3倍体积的50%乙醇,2倍体积的70%乙醇,收集洗脱液,真空干燥后得罗布麻总黄酮有效部位提取物70g;
c、称取步骤b得到的罗布麻总黄酮有效部位提取物10g,使用聚酰胺填料进行柱分离,上样量与聚酰胺质量比为1:40,洗脱溶剂为体积浓度10%?90%乙醇,梯度洗脱,收集60%?90%乙醇洗脱液,并在温度50℃下用旋转蒸发仪浓缩,真空干燥,得到槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷粗提物1.8g;
d、将步骤c得到槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷粗提物500mg加甲醇溶解,再经中试反相色谱柱色谱分离,色谱条件为:体积比18:82的乙腈?0.1%甲酸水为流动相,流速180mL/min,温度室温,保留时间为18?20min,最后分离得到所述罗布麻叶中的黄酮苷化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷260mg;
实施例1得到黄酮苷化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷为黄绿色末状固体,经HPLC分析含量大于98%,如图1所示,再经1HNMR,13CNM结构解析,如图2、图3所示,该化合物为槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷,该化合物的波谱数据:
1H?NMR(600MHz,DMSO?d6)d:3.09(2H,s,malonyl),3.18(1H,m,H?4″),3.25(1H,m,H?3″),3.26(1H,m,H?2″),3.32(1H,m,H?5″),4.00(1H,dd,J=12.0,5.4Hz,H?6″),4.20(1H,d,J=12.0Hz,H?6″),5.38(1H,d,J=7.2Hz,H?1″),6.20(1H,d,J=1.2Hz,H?6),6.40(1H,d,J=1.2Hz,H?8),6.84(1H,d,J=8.4Hz,H?5′),7.52(1H,brs,H?2′),7.52(1H,d,J=8.4Hz,H?6′),12.59(1H,brs,5?OH);[0030]13C?NMR(150MHz,DMSO?d6)d:41.2(CH2malonyl),63.6(C?6″),69.5(C?4″),73.9(C?2″,5″),76.2(C?3″),93.6(C?8),98.7(C?6),101.0(C?1″),103.9(C?10),115.2(C?2′),116.2(C?5′),121.0(C?1′),121.5(C?6′),133.2(C?3),144.8(C?3′),148.5(C?4′),156.3(C?9),156.6(C?2),161.2(C?5),164.2(C?7),166.6(COmalonyl),167.9(COmalonyl),177.3(C?4)。
实施例2
化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷的制备:
a、取干燥的罗布麻叶药材6kg,加入5倍量体积的浓度30%乙醇水溶液,在温度95℃回流提取1次,提取1h,提取后过滤,合并提取液,浓缩至无醇味,得提取物2.0kg;
b、将取步骤a得到的提取物300g,使用大孔树脂进行黄酮类成分的富集,上样浓度为0.3g/mL,药材树脂体积比为1:8,,上样流速为1BV/h,用水洗脱2个柱体积,除去水溶性杂质,洗脱液为2倍体积的30%乙醇,3倍体积的60%乙醇,收集洗脱液,真空干燥后得罗布麻总黄酮有效部位提取物68g;c、称取步骤b得到的罗布麻总黄酮有效部位提取物12g,使用聚酰胺填料进行柱分离,上样量与聚酰胺质量比为1:30,洗脱溶剂为体积浓度10%?90%乙醇,梯度洗脱,收集50%?90%乙醇洗脱液,并在温度50℃下用旋转蒸发仪浓缩,真空干燥,得到槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷粗提物2.0g;
d、将步骤c得到槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷粗提物450mg加甲醇溶解,再经中试反相色谱柱色谱分离,色谱条件为:体积比18:82的乙腈?0.1%甲酸水为流动相,流速180mL/min,温度室温,保留时间为18?20min,最后分离得到罗布麻叶中的黄酮苷化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷190mg。
实施例3
化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷的制备:
a、取干燥的罗布麻叶药材6kg,加入15倍量体积的浓度70%乙醇水溶液,在温度95℃回流提取2次,提取3h,提取后过滤,合并提取液,浓缩至无醇味,得提取物2.1kg;
b、将取步骤a得到的提取物300g,使用大孔树脂进行黄酮类成分的富集,上样浓度为0.2g/mL,药材树脂体积比为1:10,上样流速为3BV/h,用水洗脱3个柱体积,除去水溶性杂质,洗脱液为3倍体积的70%乙醇,2倍体积的30%乙醇,收集洗脱液,真空干燥后得罗布麻总黄酮有效部位提取物66g;
c、称取步骤b得到的罗布麻总黄酮有效部位提取物10g,使用聚酰胺填料进行柱分离,上样量与聚酰胺质量比为1:20,洗脱溶剂为体积浓度10%?90%乙醇,梯度洗脱,收集50%?90%乙醇洗脱液,并在温度50℃下用旋转蒸发仪浓缩,真空干燥,得到槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷粗提物1.8g;
d、将步骤c得到槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷粗提物400mg加甲醇溶解,再经中试反相色谱柱色谱分离,色谱条件为:体积比18:82的乙腈?0.1%甲酸水为流动相,流速180mL/min,温度室温,保留时间为18?20min,最后分离得到罗布麻叶中的黄酮苷化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷150mg。
实施例4
罗布麻叶中的黄酮苷类化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷对脂多糖刺激的小鼠单核巨噬细胞(RAW264.7细胞)的影响:
小鼠单核巨噬细胞(RAW264.7细胞)传代后在含10%胎牛血清(FBS)的改良Eagle培养基(DMEM)中培养,将2×104个/孔单核巨噬细胞(RAW264.7)接种于96孔板培养24h,小鼠单核巨噬细胞(RAW264.7细胞)经200?600μM的槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷处理后,除正常对照组外,其余各组均加入终浓度为1μg/mL的脂多糖,给药后培养16h后,将细胞培养板取出处理,采用CCK?8法测定细胞存活率;收集细胞上清,用酶联免疫吸附法(ELISA)试剂盒检测细胞上清肿瘤坏死因子?α(TNF?α)和白介素?6(IL?6)的含量。用亚硝酸盐测定试剂盒(Griess法)检测细胞上清中一氧化氮(NO)的含量,取各组细胞上清液50μL于96孔板中,每组做3个复孔,向每孔中加入Griess试剂Ⅰ和Griess试剂Ⅱ各50μL;用酶标仪在540nm检测吸光度;
实验结果:
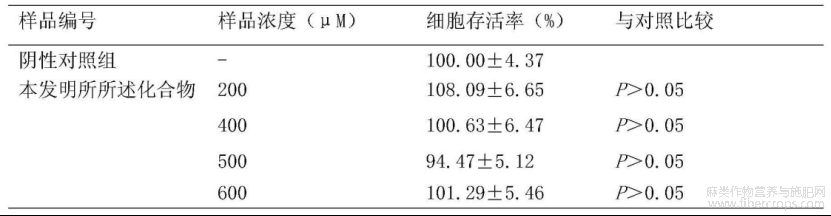
如表1,图4所示,在CCK?8试验中考察本发明提供的罗布麻叶中的黄酮苷类化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷孵育后对小鼠单核巨噬细胞(RAW264.7细胞)的细胞活力影响,结果显示:该化合物在200μM,400μM,500μM,600μM的浓度范围内均不影响小鼠单核巨噬细胞(RAW264.7细胞)的细胞活力,为实验筛选合适药物浓度提供参考;
表1 黄酮苷类化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷对小鼠单核巨噬细胞(RAW264.7细胞)细胞存活率的影响:
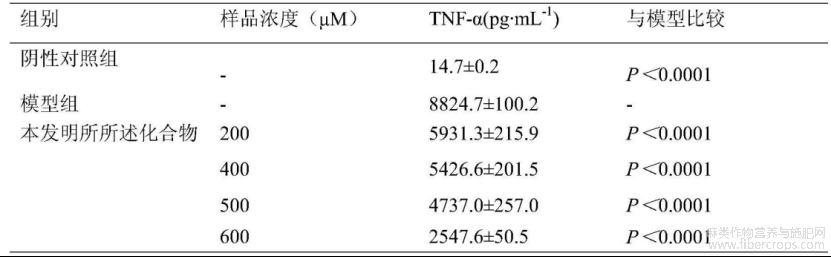
如表2?表4,图5所示,200?600μM的罗布麻叶中黄酮苷类化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷处理细胞后细胞中一氧化氮(NO)、肿瘤坏死因子?α(TNF?α)和白介素?6(IL?6)含量显著降低,说明化合物黄酮苷类化合物物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷具有显著抑制一氧化氮(NO)和炎症因子生成的活性,对一氧化氮(NO)、肿瘤坏死因子?α(TNF?α)和白介素?6(IL?6)的抑制率最高分别可达到92 .65%、71 .13%和71 .70%,说明槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷具有显著的抗炎活性;
表2 罗布麻叶中黄酮苷类化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷对脂多糖刺激的小鼠单核巨噬细胞(RAW264.7细胞)中一氧化氮(NO)含量的影响:
表3 罗布麻叶中黄酮苷类化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷对脂多糖刺激的小鼠单核巨噬细胞(RAW264.7细胞)中肿瘤坏死因子?α(TNF?α)含量的影响:
表4 罗布麻叶中黄酮苷类化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷对脂多糖刺激的小鼠单核巨噬细胞(RAW264.7细胞)中白介素?6(IL?6)含量的影响:
实施例5
罗布麻叶中黄酮苷类化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷对脂多糖刺激的小鼠小胶质细胞(BV2细胞)细胞的影响:
小鼠小胶质细胞(BV2细胞)细胞传代后在含10%胎牛血清(FBS)的改良Eagle培养基(DMEM)中培养,将6.5×104个/孔小鼠小胶质细胞(BV2细胞)细胞接种于24孔板,培养24h,小鼠小胶质细胞(BV2细胞)细胞经50?400μM的槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷处理后,除正常对照组外,其余各组均加入终浓度为1μg/mL的脂多糖,培养24h后,将细胞培养板取出处理;用亚硝酸盐测定试剂盒(Griess)法检测细胞上清中一氧化氮(NO)的含量,取各组细胞上清液50μL于96孔板中,每组做3个复孔,向每孔中加入Griess试剂Ⅰ和Griess试剂Ⅱ各50μL;用酶标仪在540nm检测吸光度,计算细胞上清一氧化氮(NO)的含量;
实验结果:
如表5,图6所示,在CCK?8试验中考察本发明提供的罗布麻叶中黄酮苷类化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷孵育后对小鼠小胶质细胞(BV2细胞)细胞活力影响,结果显示:该化合物在50μM,100μM,200μM,400μM的浓度范围内均不影响小鼠小胶质细胞(BV2细胞)的细胞活力,为实验筛选合适药物浓度提供参考;
表5 罗布麻叶中黄酮苷类化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷对小鼠小胶质细胞(BV2细胞)细胞存活率的影响:
如表6,图7所示,50?400μM的罗布麻叶中黄酮苷类化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷处理细胞后细胞中一氧化氮(NO)含量显著降低,说明罗布麻叶中黄酮苷类化合物物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷具有显著抑制一氧化氮(NO)生成的活性,在100μM浓度时一氧化氮(NO)抑制率可达43.19%,且随着浓度提高其抑制率也随之升高,当浓度为400μM时,对一氧化氮(NO)含量的抑制率可达到94.21%,说明槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷具有显著的抗炎活性;
表6 罗布麻叶中黄酮苷类化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷对脂多糖刺激的小鼠小胶质细胞(BV2细胞)细胞中一氧化氮(NO)含量的影响:
本发明所述的黄酮苷类化合物槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷可明显降低脂多糖刺激的小鼠小胶质细胞(BV2细胞)细胞中一氧化氮(NO)含量,说明槲皮素?3?O?(6”?O?丙二酰基)?β?D?葡萄糖苷具有显著的抗炎活性。具有抗炎活性功效的保健品中的用途。