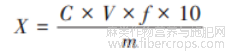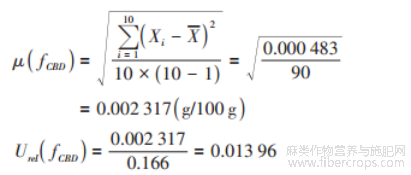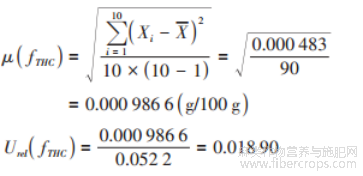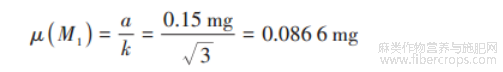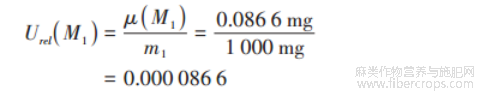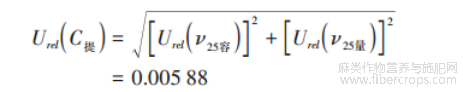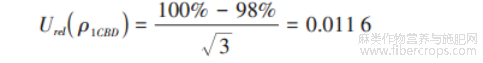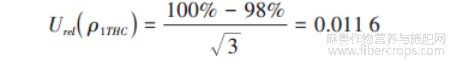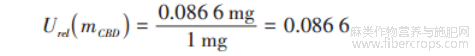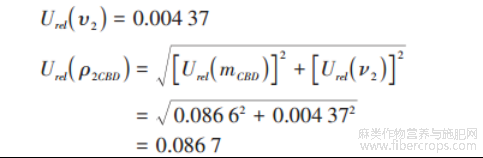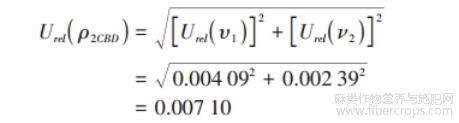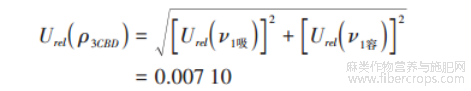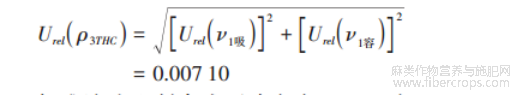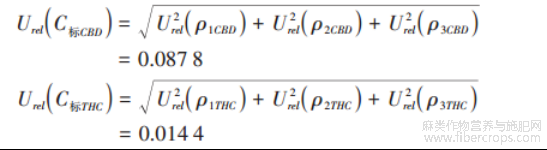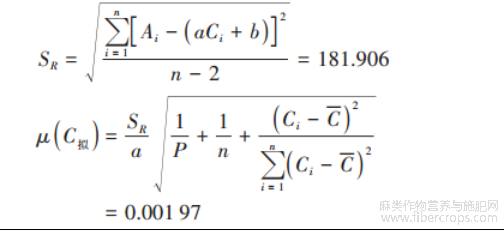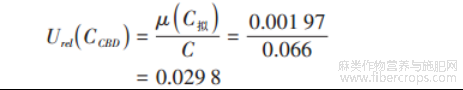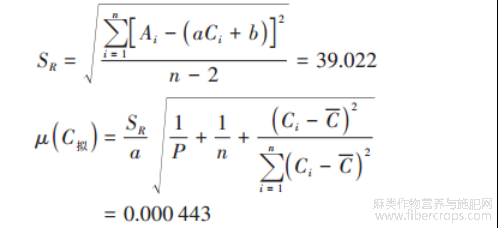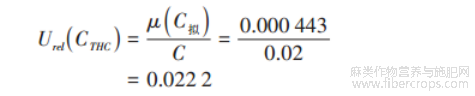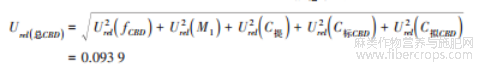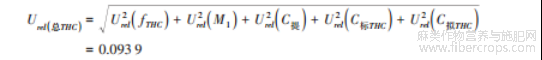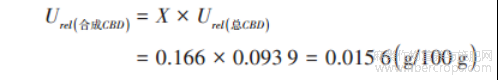摘 要:对采用高效液相色谱法(HPLC)测定工业大麻中大麻二酚(CBD)和四氢大麻酚(THC)的不确定度进行评估,依据《测量不确定度评定与表示》(JJF1059.1-2012)和《化学分析中不确定度的评估指南》(CNAS-GL006-2019),建立了HPLC法测定工业大麻中CBD和THC的不确定度评定的数学模型,逐层对测定过程中各不确定度来源进行分析,对各不确定度分量进行计算,再对测定结果进行合成不确定度和扩展不确定度评估。结果表明,检测CBD过程中,不确定度来源的主要因素所占分量由大到小排序为:标准溶液配制>标准工作曲线拟合>重复次数>提取>样品称量;检测THC过程中,不确定度来源的主要因素所占分量由大到小排序为:标准工作曲线拟合>重复次数>标准溶液配制>提取>样品称量。CBD结果平均值为0.166g/100g,扩展不确定度为0.0312g/100g,取值结果为X=(0.166±0.0312)g/100g,包含因子k=2;THC平均值为0.0522g/100g,扩展不确定度为0.00344g/100g,取值结果为X=(0.0522±0.00344)g/100g,包含因子k=2。此方法适用于类似条件下CBD和THC测定不确定度的评定。
关键词:不确定度评定;工业大麻;大麻二酚;四氢大麻酚;高效液相色谱法
工业大麻又称大麻、火麻和汉麻[1],允许种植的大麻品种为四氢大麻酚(THC)含量小于0.3%。目前应用于纺织、食品、化妆品和制药等多种行业,应用范围广,经济价值大[2-7]。大麻叶中含有多种大麻酚类衍生物,已分离到15种以上,最主要且含量较高的是大麻二酚和四氢大麻酚[8]。具有止痛、抗炎、安眠、镇痉和镇静等作用[9-15]。大麻二酚是工业大麻品质评价的重要指标,四氢大麻酚是工业大麻质量控制的重要指标,为了确保检测结果可信,对工业大麻中大麻二酚和四氢大麻酚检测技术进行不确定度评定尤为重要。
测量不确定度评定与检测结果的合格判定直接相关[16],对量值溯源和方法确认具有重要意义[17]。《检测和校准实验室能力的通用要求》(GB/T 27025-2019)明确规定[18],当检测结果处于临界值或客户有需求时,须提供检测结果的不确定度。
本研究依据《化学分析中不确定度的评估指南》(CNAS-GL006-2019)和《测量不确定度评定与表示》(JJF 1059.1-2012)规定的方法,对HPLC法测定大麻中CBD和THC的不确定度进行评定,分析影响测定结果准确性的各种因素,旨在相关检测过程中,尽可能控制不准确性因素的影响,以提高检测结果的准确性。
1 材料与方法
1.1 材料
整株工业大麻,由吉林省农业科学院、吉林省麻类工程研究中心和吉林省麻类科技创新中心提供。
1.2 试剂
四氢大麻酚(THC)标准溶液(浓度1.0 mg/mL)和大麻二酚(CBD)标准品(浓度1.0 mg/mL)(美国Sigma-Aldrich公司),乙腈、甲醇和色谱纯(美国Thermo Fisher公司),95%乙醇,分析纯(上海国药集团),试验用水均为超纯水,0.45μm滤膜(丹东百特仪器有限公司)。
1.3 仪器
1260Ⅱ高效液相色谱仪:安捷伦有限公司;VF 611超纯水系统:德国 SARTORIUS公司;BT 124S电子天平(±0.001g):中国赛多利斯科学仪器(北京)有限公司。
1.4 方法
1.4.1 待测液制备
称取100目的试样1g(精确至0.01g)于回流瓶中,加入20mL 95%乙醇回流60min,重复一次,合并两次提取液,过滤,减压回收乙醇,用甲醇溶解转移至25mL容量瓶中,定容至刻度,摇匀,过0.45μm滤膜,上机测定。
1.4.2 标准储备液配制
大麻二酚标准储备液:准确称取大麻二酚(CBD标准品:1.0mg,用2mL甲醇溶解,制成0.5mg/mL标准储备液。于2~4℃条件下储存,有效期为1年。
四氢大麻酚标准储备液:准确吸取1mg/mL的四氢大麻酚标准溶液0.5mL于5 mL容量瓶中,用甲醇定容至刻度,制成0.1mg/mL的标准储备液。于-20℃条件下储存,有效期为3年。
1.4.3 标准工作液配制
大麻二酚标准工作液:吸取适当体积的大麻二酚标准储备液,用甲醇逐级稀释,配制成0.02mg/mL、0.04 mg/mL、0.05mg/mL、0.06mg/mL、0.08mg/mL、0.10mg/mL的标准工作液。于2~4℃条件下储存,有效期为1个月。
四氢大麻酚标准工作液:吸取适当体积的四氢大麻酚标准储备液,用甲醇逐级稀释,配制成0.002 mg/mL、0.004 mg/mL、0.006 mg/mL、0.008 mg/mL、0.010 mg/mL、0.020mg/mL、0.040 mg/mL、0.060mg/mL、0.080mg/mL、0.10mg/mL的标准工作液。于-20℃条件下储存,有效期为6个月。
1.4.4 色谱条件
色谱柱:C18柱,柱长150 mm,内径4.6 mm,粒度3.5μm;或者性能相当的色谱柱。
柱温:35℃。
流动相:乙腈-水(68∶32,v/v)。
流动相流速:1.0mL/min。
进样体积:10μL。
1.5 数学模型的建立
大麻二酚和四氢大麻酚含量计算公式:
式中:X为试样中大麻二酚和四氢大麻酚含量(g/100g),C 为标准曲线上查得大麻二酚和四氢大麻酚的浓度(mg/mL),V为试样定容体积(mL),m为试样质量(g),f为稀释倍数;10为单位换算。
2 结果与分析
2.1 来源分析
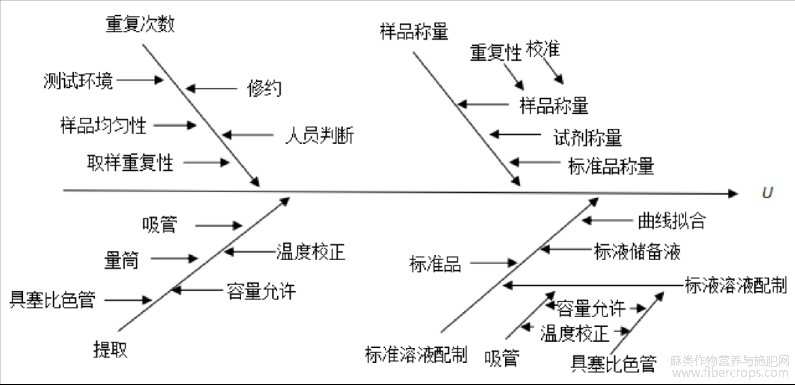
根据 JJF 1059.1-2012《测量不确定度评定与表示》[19],按照检测流程和数学模型,不确定度的来源见图1。
(1)重复次数引入的不确定度 Urel(f);
(2)样品称量引入的不确定度 Urel(M1);
(3)提取过程引入的不确定度 Urel(C提);
(4)标准溶液配制引入的不确定度 Urel(C标);
(5)标准工作曲线拟合求浓度引入的不确定度 Urel(C拟)。
图1 不确定度来源与分析
2.2 不确定度分量的评定
2.2.1 重复次数引入的不确定度Urel(f)
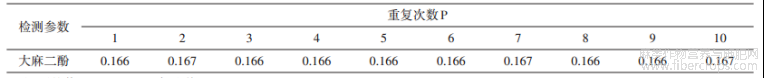
采用同一大麻样品、同一检验员、同一台仪器重复处理测定10次,用标准偏差评定重复次数引入的不确定度,测定结果见表1和表2。
由表1计算大麻二酚μ(fCBD)和 Urel(fCBD)为:
表1 大麻中大麻二酚含量测定结果
注:平均值:0.166g/100g,标准偏差:0.000483g/100g
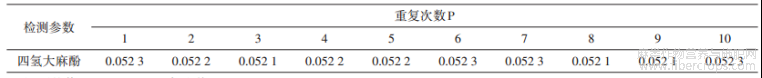
表2 大麻中四氢大麻酚含量测定结果
注:平均值:0.0522g/100g,标准偏差:0.0000876g/100g
由表2计算四氢大麻酚μ(fTHC)和U(fTHC)为:
2.2.2样品称量引入的不确定度U(M)
样品称量引入的不确定度主要是电子天平。电子天平最大允许误差为+0.15 mg,按矩形分布计算,则电子天平引人的不确定度μ(M,)为:
电子天平引人的相对不确定度 U.(M,)为:
2.2.3 提取过程引入的不确定度U.(C”)
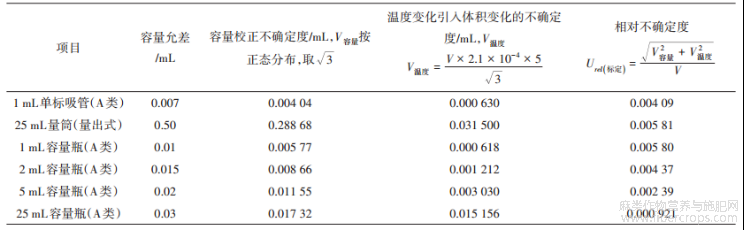
提取过程中引人的不确定度主要是容量器具(25m量筒和25m容量瓶,根据 JG 196-2006《常用玻璃量器》…,其不确定度和相对不确定度计算结果见表3。
2.2.4 标准溶液配制引入的不确定度 Urel(C 标)
2.2.4.1 标准品纯度引入的不确定度 Urel(ρ1)
由大麻二酚标准物质证书可知,标准品纯度≥ 98%,按正态分布计算,取3。标准品纯度不确定度 Urel(ρ1CBD)为:
由四氢大麻酚标准物质证书可知,标准品纯度≥98%,按正态分布计算,取3。标准品纯度不确定度 Urel(ρ1THC)为:
2.2.4.2 标准储备液引入的不确定度 Urel(ρ2)
称量 1.0 mg 大麻二酚引入的相对不确定度Urel(mCBD),计算方法同 2.2.2。
配制大麻二酚标准储备液使用 2 mL 容量瓶,引入的相对不确定度 Urel(V2() 见表 3)。
配制四氢大麻酚标准储备液使用1 mL单标吸管和5 mL容量瓶,引入的相对不确定度Urel(THC)见表3。
2.2.4.3 标准工作液配制引入的不确定度Urel(ρ3)
配制标准溶液过程中使用1mL单标吸管和1mL容量瓶,各自引入的相对不确定度见表3。配制大麻二酚标准工作液引入的相对不确定度Urel(ρ3CBD)为:
配制四氢大麻酚标准工作液引入的相对不确定度Urel(ρ3THC)为:
标准溶液配制合成不确定度Urel(C 标)为:
2.2.5 标准工作曲线拟合求浓度引入的不确定度Urel(C拟)
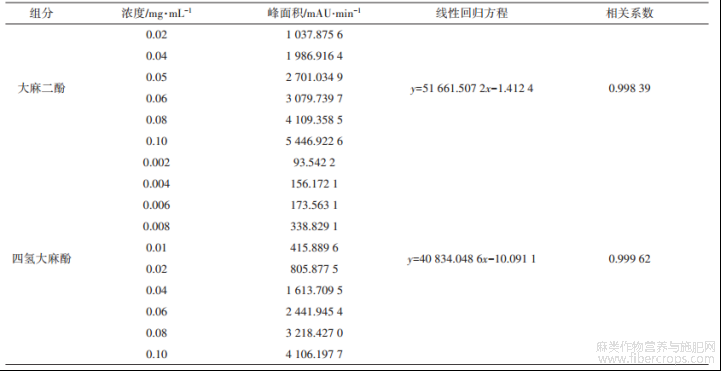
大麻二酚采用6个浓度水平的标准溶液进行测定。四氢大麻酚采用10个浓度水平的标准溶液进行测定。相应的峰面积与标准溶液浓度用最小二乘法进行拟合,结果见表4。
表4 最小二乘法拟合标准曲线数据
拟合曲线求样品溶液中大麻二酚平均浓度产生的标准不确定度为μ(C 拟):
式中:SR为标准溶液峰面积的标准偏差,Ai为各溶液峰面积,C为样品溶液的平均质量浓度,C为标准系列溶液的平均质量浓度,Ci为各标准溶液浓度值,a为回归方程斜率,b为截距,P为样品平行测定次数,n为标准工作曲线的点数。
大麻二酚最小二乘法拟合标准曲线求样品浓度引入的相对不确定度 Urel(CCBD)为:
拟合曲线求样品溶液中四氢大麻酚平均浓度产生的标准不确定度为μ(C 拟):
四氢大麻酚最小二乘法拟合标准曲线求样品浓度引入的相对不确定度 Urel(CTHC)为:
2.3 大麻中大麻二酚和四氢大麻酚含量测定的合成不确定度和扩展不确定度
大麻二酚合成不确定度 Urel(总 CBD)为:
四氢大麻酚合成不确定度 Urel(总 THC)为:
大麻中大麻二酚含量为 0.166 g/100 g,合成标准不确定度为:
大麻中四氢大麻酚含量为 0.052 2 g/100 g,合成标准不确定度为:
2.4 不确定度分量影响比较各不确定度分量的比较结果见图2和图3。
图2 大麻二酚合成相对不确定度分量比较
图3 四氢大麻酚合成相对不确定度分量比较
3 结论
CBD结果平均值为0.166g/100g,扩展不确定度为0.0312g/100 g,取值结果为X=(0.166±0.0312)g/100g;THC结果平均值为0.0522g/100g,扩展不确定度为0.00344g/100g,取值结果为X=(0.0522±0.00344)g/100g。
测定CBD过程中引入不确定度的各分量影响因素排序为:标准溶液配制>标准工作曲线拟合>重复次数>提取>样品称量;测定THC过程中引入不确定度的各分量影响因素排序为:标准工作曲线拟合>重复次数>标准溶液配制>提取>样品称量。
参考文献
[1]高哲,张志军,李晓君,等.火麻叶中大麻二酚的热回流提取工艺研究[J].中国油脂,2019,44(3):107-111.
[2]陈建华,臧巩固,赵立宁,等.大麻化学成分研究进展与开发我国大麻资源的探讨[J].中国麻业,2003(6):6-11.
[3]卢延旭,董鹏,崔晓光,等.工业大麻与毒品大麻的区别及其可利用价值[J].中国药理学通报,2007(8):1112-1114.
[4]刘胜贵,马海悦,李智高,等.HPLC法测定工业大麻中CBD和THC的含量[J].云南化工,2020,47(5):62-64.
[5]李杨,赵晓俊,王璞,等.工业大麻中4种大麻素脱羧工艺研究[J].中国麻业科学,2023,45(1):20-24.
[6]张雪,徐立群,王庆峰,等.不同用途亚麻的研究进展[J].东北农业科学,2018,43(5):16-20.
[7]赵国良,张喜平,卜虎虎,等.天水生态条件下不同大麻品种(系)产量及株高生长研究[J].东北农业科学,2022,47(3):59-64.
[8]郝红江,孙武兴,邢俊波,等.工业大麻叶提取大麻二酚工艺研究[J].绿色科技,2019(20):149-150.
[9]车野,郭丽,王明泽,等 . 我国工业大麻发展现状及存在的问题[J]. 黑龙江农业科学,2022(9):105-110.
[10]成亮,孔德 .大麻中非成瘾性成分大麻二酚及其类似物的研究概况[J]. 中草药,2008,39(5):783-787.
[11]徐雯,张敬军.大麻二酚治疗癫痫的研究进展[J].山东第一医科大学(山东省医学科学院)学报,2022,43(1):74-77.
[12]王秋月,卢芳,刘树民,等.大麻及大麻素药用价值的现代研究进展[J].中药药理与临床,2020,36(4):222-227.
[13]殷莎,唐双奇,陆阳,等.大麻二酚神经保护作用机制研究进展[J].中草药,2014,45(3):432-436.
[14]李臻,王雁,KwanPatrick.大麻二酚在癫痫治疗中的研究进展[J].中华神经科杂志,2019,52(7):586-591.
[15]胡乃华.大麻中抗癫痫作用新化合物的发现[J].天然产物研究与开发,2021,33(11):1917.
[16]吴迪,江涛,李长燕,等.超高效液相色谱-串联质谱法测定鱼肉中4种有机磷农药残留量不确定度评定[J].东北农业科学,2024,49(3):102-108.
[17]刁银军,刘莉,肖珊美,等.UPLC-MS/MS法测定元胡中4种有机磷农药残留的不确定度评定[J].安徽农业科学,2018,46(6):157-161.
[18]国家市场监督管理总局,国家标准化管理委员会.检测和校准实验室能力的通用要求:GB/T27025—2019[S].北京:中国标准出版社,2020.
[19]国家市场监督管理总局.中华人民共和国国家计量技术规范JJF1059-2012测量不确定度评定与表示[S].北京:中国质检出版社,2013.
[20] 全国流量容量计量技术委员会 .JJG 196-2006 中华人民共和国国家计量检定规程常用玻璃量器[S]. 北京:中国计量出版社,2007.
文章摘自:张鑫,刘丽宅,王多伽,等.HPLC法测定工业大麻中大麻二酚和四氢大麻酚的不确定度评定[J].东北农业科学,2024,49(05):81-86.